電気とはそもそもどんな現象?(電気の基礎知識)

消防設備士、
電気工事士と電気を扱う資格には欠かせない
電気というものについての基礎知識!
理論を頭に詰め込むのではなく、
理解から始めればイメージが頭に浮かぶようになるので
勉強に、そして実務にも役立ちます!
「そもそも電気とは何?」
まずはここから始めていきましょう!
原子の構成
学校の理科の授業で習った原子。
みなさん懐かしいのでは?
学生の方だと勉強中だったりちょっと前にやっていると思います。
昔の復習がてら理解を深めていただければと思います。
電気の素はこの原子なので、
構成をしっかり頭にイメージしましょう!
原子とは、
太陽を中心に回る地球や火星をイメージしていただけると
わかりやすいと思います。
太陽の部分に原子核。
地球や火星の位置に電子があります。
原子核は陽子と中性子がくっついたものです。
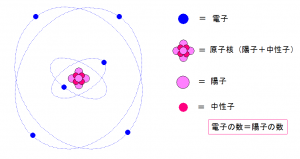
物質を構成する最少単位です。
陽子、中性子、電子はそれぞれ元素ごとに数が決まっていて、
陽子の数が原子番号になっています。
原子番号1 水素=陽子数1
原子番号2 ヘリウム=陽子数2
原子番号3 リチウム=陽子数3
といった具合です。
陽子と電子の数は必ず同数で、
中性子は元素によってバラバラです。
この3つの素粒子、特に陽子が何個あるかによって
元素の性質が変わります。
陽子と電子が1つずつなら水素ですが、
これが26個になれば鉄に。
不思議ですよね。
電荷とは?
陽子と電子は、
その1つ1つに電気的なエネルギーを持っています。
この、陽子と電子が持つ
電気的な性質のことを「電荷」といいます。
陽子は正のエネルギー(+)=正電荷、
電子は負のエネルギー(-)=負電荷。
中性子は中性で電気的なエネルギーは持っていません。
1つの電子が持っている電荷を素電荷といい、
電荷の最小単位です。
水素の正電荷は1、負電荷も1、
鉄の正電荷は26、負電荷も26。
といった具合ですね。
原子は、
陽子数と電子数が同数で、
それぞれの(+)と(-)のエネルギーが打ち消しあっているので
電気的に中性になります。
クーロン力
電荷は、
磁石と同じように異極同士は引き合い、
同極同士は反発しあうという性質を持っています。
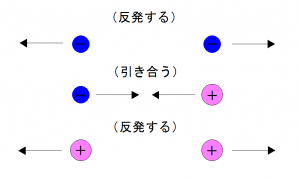
マイナスとマイナス、
プラスとプラスは反発。
マイナスとプラスは引き付けあいます。
なので、
中心にある陽子が持っているプラスのエネルギーに
マイナスのエネルギーを持つ電子が引き付けられているというイメージですね!
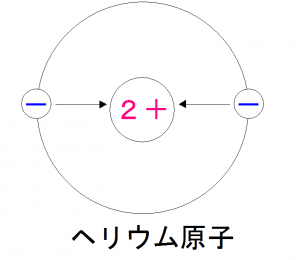
では、
「なぜ中心にある陽子同士は反発しないでくっついていられるの?」
と疑問を持ちませんか?
物理の世界には、
「重力」、「電磁力」、「強い力」、「弱い力」という4つの力があるそうで、
この陽子同士が反発せずにくっついていられる力。
それが「強い力」と呼ばれるものだそうです。
(電磁的な反発力をものともしない力で強い力というそうです)
興味のある方は、
ぜひ物理の勉強を!
自由電子
中心にある陽子に引き寄せられている電子
というイメージでしたが、
電子が周回軌道を描く電子殻の一番外側では
電子を引き付ける力がそれほど強くないものがあり、
外部から刺激を受けることにより
簡単に周回軌道から飛び出してしまうものがあります。
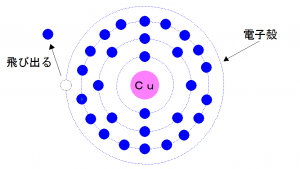
この飛び出た電子を、
「自由電子」といい、
電子が飛び出てしまった原子は、
マイナスのエネルギーを失うのでプラスのエネルギーが強くなり
プラスに帯電します。
一方、
自由電子の方は電子そのものがマイナスに帯電しているため、
他の原子にくっつくことにより、電子が1つ増えた原子はマイナスに帯電します。
電気とは、
この自由電子の移動によって起こる現象なのです。
ちなみに、
電子が周回軌道を飛び出しやすいものを導体といい、
電気を非常に通しやすいものです。
銅やアルミニウムといった金属に多いです。
逆に、
結束力が強すぎて電子が飛び出しにくいものを絶縁体といい、
これらは全く電気を通しません。
こちらは、
また別の機会にご紹介します。
次は、
電流についてご紹介していきたいと思います。
電流とは?(電気の基礎知識)








